FlowJo v10 中文教程:从入门到精通
第一部分:FlowJo 核心概念
在开始操作之前,理解 FlowJo 的几个核心概念至关重要,这会让你的分析之路事半功倍。
-
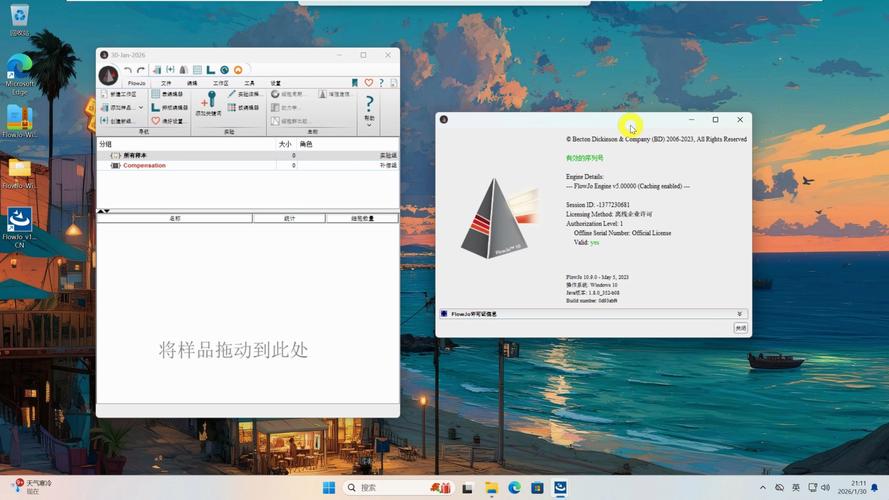
工作区
- 是什么: FlowJo 的主界面,是你进行所有分析的地方。
- 包含: 左侧是实验节点树,中间是样本列表,右侧是分析视图(图表和表格)。
-
实验节点树
- 是什么: 位于工作区左侧,以树状结构展示了你的所有实验。
- 结构:
- 顶级节点: 你的实验文件夹或数据来源。
- 实验节点: 一个完整的实验,包含所有样本和它们对应的
.fcs文件。 - 样本节点: 单个的
.fcs文件,是你分析的基本单位。 - 群体: 你在样本中根据 gating 策略定义的细胞亚群,群体是 FlowJo 的核心,它包含了 gating 路径和统计数据。
-
样本
- 是什么: 一个
.fcs(Flow Cytometry Standard) 文件,包含了流式细胞仪采集到的所有细胞事件(数据点)。
- 是什么: 一个
-
群体
 (图片来源网络,侵删)
(图片来源网络,侵删)- 是什么: 通过在图上画门而定义的细胞亚群,从“淋巴细胞门”中再分出“T细胞门”。
- 层级关系: 群体具有父子关系,子群体的统计数据(如细胞数、百分比)是基于其父群体的。
-
Gating 策略
- 是什么: 一系列连续的 gating 操作,用于从原始数据中一步步筛选出你感兴趣的细胞群,一个好的 gating 策略应该是清晰、可重复的。
-
模板
- 是什么: 一个应用了特定 gating 策略和图表设置的样本,你可以将这个模板应用到其他具有相同标记的样本上,实现批量、标准化的分析。
第二部分:基础操作流程
本部分将带你走完一个完整的流式数据分析流程。
步骤 1:导入数据
- 打开 FlowJo,进入工作区。
- 点击菜单栏的
File->Import->Folder...。 - 在弹出的窗口中,选择包含你所有
.fcs文件的文件夹,FlowJo 会自动扫描该文件夹下的所有.fcs文件。 - 命名你的实验:在 "Workspace Name" 中给你的实验起一个名字,"小鼠脾脏淋巴细胞分析"。
- 点击
OK,FlowJo 会将文件夹下的所有.fcs文件作为样本导入实验节点树中。
步骤 2:初步查看和补偿
- 查看样本: 在左侧的实验节点树中,双击任意一个样本节点,中间的样本列表会显示该样本的详细信息,右侧会自动弹出第一个参数的直方图图。
- 设置补偿:
- 流式细胞仪使用不同颜色的激光检测不同荧光,但荧光之间可能会有光谱重叠,需要进行补偿校正。
- 单染管: 你需要有用于补偿的单染样本(每个管只标记一种抗体)。
- 在实验节点树中,按住
Ctrl或Cmd键,同时选中所有单染管和未染管。 - 右键点击选中的样本,选择
Create Compensation Matrix。 - FlowJo 会自动识别单染管,并计算一个补偿矩阵,检查一下 "Compensation" 窗口中的图,确保每个单染管的阳性峰都正确地落在其自己的轴上。
- 点击
Apply,将这个补偿矩阵应用到所有选中的样本(通常也包括你的实验样本)。
步骤 3:Gating 分群(核心步骤)
我们以一个典型的淋巴细胞免疫分型为例:

-
选择起始样本: 选择一个代表性的样本(通常是阳性对照或样本组中的一个)开始 gating,完成一个样本的 gating 策略后,可以将其作为模板应用到其他样本。
-
画第一道门 - FSC-A vs SSC-A (排除碎片和死细胞)
- 在右侧视图中,点击
Graphs标签,选择FSC-A(前向角散射,反映细胞大小) 和SSC-A(侧向角散射,反映细胞颗粒度)。 - 在图上画一个“P1”门,圈出细胞分布集中的区域,通常是淋巴细胞群。
- 双击这个门,命名为 "Lymphocytes" (淋巴细胞)。
- 在右侧视图中,点击
-
画第二道门 - Singlets (排除粘连细胞)
- 为了排除两个或多个细胞粘在一起的情况,我们需要看双联体/三联体。
- 点击
Graphs标签,选择FSC-H(高度) 和FSC-W(宽度)。 - 在图上画一个“P2”门,圈出对角线上单个细胞的区域。
- 双击命名为 "Singlets" (单细胞)。
- 关键操作: 右键点击 "Singlets" 群体,选择
Subset->Parent,你的分析对象就从 "All Events" 变成了 "Singlets" 群体。
-
画第三道门 - Live/Dead Cells (排除死细胞)
- 如果你的实验使用了染死细胞的染料(如 Zombie Aqua, DAPI),这一步非常重要。
- 点击
Graphs标签,选择FSC-A和你的死细胞染料通道(如Aqua-A)。 - 在活细胞区域画一个门,圈出染料阴性的细胞。
- 双击命名为 "Live Cells" (活细胞)。
- 同样,右键点击 "Live Cells",选择
Subset->Parent。
-
画第四道门 - 主要细胞亚群 (如 T, B, NK 细胞)
- 现在我们的分析对象是 "Live Singlets"。
- 点击
Graphs标签,选择CD3(T细胞标志物) 和CD19(B细胞标志物)。 - 你会看到四个象限:
CD3+ CD19-: T 细胞CD3- CD19+: B 细胞CD3- CD19-: 可能是 NK 细胞或其他细胞
- 使用
Quadrant工具(工具栏上的十字图标)来画象限门。 - 依次双击每个象限,命名为 "T cells", "B cells", "NK cells"。
步骤 4:创建图表
- 选择图表类型: 在右侧工具栏或菜单栏
Graphs中,选择你想要的图表类型,如Dot Plot(点图),Contour Plot(等高线图),Histogram(直方图)。 - 选择要展示的群体和参数:
- 在左侧的实验节点树中,按住
Shift键,依次点击你想要展示的群体("T cells", "B cells", "NK cells")。 - 在右侧的图表区域,点击
X和Y轴的下拉菜单,选择你想要分析的参数(CD4和CD8)。 - FlowJo 会自动为每个群体生成一张图表。
- 在左侧的实验节点树中,按住
步骤 5:创建并应用模板
-
创建模板:
- 在左侧实验节点树中,右键点击你已经完成 gating 的起始样本。
- 选择
Create Template。 - 在弹出的窗口中,勾选你想要包含在模板中的所有群体(从 "Lymphocytes" 到最后的 "NK cells" 等)。
- 点击
OK,该样本节点旁边会出现一个模板图标。
-
应用模板:
- 在左侧实验节点树中,按住
Shift键,选中所有你想要应用此模板的样本。 - 右键点击选中的样本,选择
Apply Template。 - 选择你刚刚创建的模板,点击
OK。 - FlowJo 会自动为所有选中的样本执行相同的 gating 策略,并生成相应的图表和统计数据。
- 在左侧实验节点树中,按住
步骤 6:查看和导出结果
- 查看统计数据: 在右侧视图下方,点击
Table标签,FlowJo 会自动生成一个表格,显示每个样本、每个群体的细胞数和百分比。 - 导出图表:
- 右键点击你想要导出的图表,选择
Export->Graph as Image...。 - 可以选择导出为
PNG,TIFF,JPG等格式,设置分辨率和尺寸。
- 右键点击你想要导出的图表,选择
- 导出表格:
- 右键点击
Table标签页,选择Export->Table as Excel...或Table as Text...。 - 可以轻松地将数据导出到 Excel 进行后续统计分析。
- 右键点击
- 生成报告:
- FlowJo 可以生成专业的 PDF 报告,通过
Report功能,可以自定义报告的布局、包含哪些图表和表格。
- FlowJo 可以生成专业的 PDF 报告,通过
第三部分:高级功能与技巧
当你掌握了基础操作后,可以探索以下高级功能,它们能极大地提升你的分析效率和深度。
-
群组
- 是什么: 将功能相似的样本(如同一处理组的所有小鼠)组织在一起。
- 用途: 方便进行组间比较,统计图表会自动按组显示不同颜色。
- 操作: 在实验节点树中,选中要归为一组的样本,右键选择
Group->New Group...,然后命名。
-
平台
- 是什么: 一个更高级的群组,用于管理不同标记组合但实验目的相同的样本。
- 用途: 当你有多组样本,每组使用了不同的抗体面板时,平台可以帮你统一管理这些不同的实验。
-
统计
- 是什么: FlowJo 内置了丰富的统计工具。
- 操作: 右键点击一个群体,选择
Statistics->Add Statistics,可以添加Median,Mean,Geometric Mean,% of Parent,% of Grandparent等指标到表格中。
-
串联门
- 是什么: 一个群体,其定义依赖于另一个样本的 gating 结果,用某个荧光微球(bead)的标准曲线来设定另一个样本的阳性阈值。
- 用途: 用于实现跨样本的标准化 gating。
-
脚本与插件
- 是什么: FlowJo 支持使用 JavaScript 编写脚本,实现高度自动化的分析流程。
- 用途: 对于重复性极高、步骤复杂的分析,编写脚本可以一劳永逸,一些第三方插件(如 OpenCyto, t-SNE)也通过脚本形式扩展了 FlowJo 的功能。
第四部分:学习资源推荐
-
FlowJo 官方资源(英文,但质量最高):
- 官方文档: https://docs.flowjo.com/ - 最权威的参考手册。
- 官方博客: https://blog.flowjo.com/ - 包含大量技巧、教程和行业新闻。
- YouTube 频道: 搜索 "FlowJo LLC",有大量视频教程,从入门到高级应有尽有。
-
中文社区与资源:
- Bilibili (B站): 搜索 "FlowJo 教程",有很多国内用户分享的视频教程,非常直观。
- 微信公众号: 关注一些生物信息学或流式细胞术相关的公众号,有时会推送 FlowJo 的使用技巧。
- 专业论坛: 在丁香通、小木虫等生物科研论坛的流式细胞版块,可以提问和交流。
学习 FlowJo 的最佳路径是:理解核心概念 -> 跟随教程动手操作 -> 分析自己的真实数据 -> 探索高级功能,不要害怕尝试,FlowJo 的操作是“非破坏性”的,你可以随时撤销 gating 操作,祝你学习顺利!